动物研究所合作揭示“铁衰老”通路及干预策略
衰老是慢性疾病的首要风险因素。半个多世纪前提出的“自由基衰老理论”将氧化损伤与衰老联系起来,在衰老研究中产生了深远影响。然而,基于该理论的广谱抗氧化干预与健康获益之间的关联尚存争议,促使学界重新审视这一问题的答案:是否存在核心的分子通路,将氧化应激与机体的系统性衰退相偶联?能否基于新的机制认知,锁定可靶向干预的关键节点,实现有效的衰老延缓?
2026年3月11日,中国科学院动物研究所刘光慧研究组、曲静研究组,联合中国科学院北京基因组研究所张维绮研究组,在Cell Metabolism发表题为“Vitamin C inhibits ACSL4 to alleviate ferro-aging in primates”的研究论文。该研究首次提出并系统阐述的是一种由铁过载触发、长链脂酰辅酶A合成酶家族成员4(ACSL4)驱动、脂质过氧化介导的衰老程序化通路,并将其命名为“铁衰老(Ferro-aging)”。这一发现为理解氧化损伤与衰老的关系提供了更精细的分子框架,也为衰老干预开辟了新路径。
与既往聚焦于铁依赖的急性细胞死亡的研究不同,这项工作的核心在于揭示铁代谢失衡可驱动一种慢性、低度的细胞功能衰退过程。研究人员将这一状态命名为“铁衰老”,从概念上区别于急性细胞死亡事件。在铁衰老进程中,ACSL4驱动的脂质过氧化构成核心驱动轴,而机体内在的抗氧化系统则构成防御屏障。这一过程广泛存在于不同分裂能力的细胞类型中,即在增殖性的干细胞和终末分化的神经元中均可观察到铁衰老特征,提示该通路具有普遍的细胞学基础。这一概念的提出,将铁生物学从“细胞如何死亡”的视角,延伸至“细胞如何老去”的新维度。
为验证这一概念,研究团队首先在人类细胞衰老模型和自然衰老灵长类模型中观察到,衰老细胞及老年灵长类多组织器官存在显著铁蓄积,并伴有脂质过氧化水平升高。在现象观察的基础上,团队进一步通过构建慢性高铁饮食小鼠模型验证因果关系,发现年轻小鼠连续饲喂高铁饲料2个月后,出现认知功能下降、运动能力减退等多系统功能衰退,表明长期铁摄入过量足以驱动多器官衰老表型。
机制解析锁定ACSL4为铁衰老的核心执行者。其在衰老细胞和多组织中表达上调,催化多不饱和脂肪酸酯化,促进脂质过氧化底物生成,将铁过载与氧化损伤紧密偶联。基于跨组织转录组分析,团队构建铁衰老特征基因集,其评分与组织衰老程度良好相关,为铁衰老的量化评估提供分子工具。从啮齿类到非人灵长类再到人类,铁衰老相关分子特征在不同物种间呈现一定保守性,提示该通路可能构成哺乳动物衰老的共性机制。
在鉴定ACSL4为核心靶标基础上,团队进一步筛选可干预铁衰老的小分子药物。通过系统评估,发现维生素C能有效抑制ACSL4活性。分子互作揭示维生素C直接结合ACSL4蛋白特定口袋,抑制其酶活性,减少促氧化脂质合成。同时,维生素C还能激活抗氧化调控因子NRF2通路,增强细胞内在抗氧化防御能力,形成双重保护机制。这一发现将一个广谱的抗氧化剂重新定义为具有明确分子靶点的酶抑制剂,揭示了维生素C通过直接靶向ACSL4发挥抗衰老作用的新机制。
在动物层面,团队探索了靶向ACSL4的基因治疗策略:利用基于CRISPR-Cas9的基因治疗载体,在老年小鼠通过静脉注射特异敲低肝脏中Acsl4基因。基因治疗干预不仅改善肝脏及多组织器官的衰老状态,还显著提升老年小鼠的认知能力和运动协调性,证明以肝脏为靶器官的ACSL4基因治疗是一种可行的衰老干预策略。这一“外周器官干预—系统性获益”的现象提示,通过延缓核心器官的衰老可能带来多系统功能改善。
为验证干预策略在高等动物中的效果,研究团队开展为期40个月的非人灵长类干预实验。非人灵长类与人类相似,自身无法合成维生素C,因此在该模型中验证维生素C的干预效果具有独特的转化价值。长期口服治疗剂量维生素C耐受性良好,显著降低老年猴子多组织中铁衰老相关分子特征及炎症水平。基于多器官表观遗传、转录组和代谢组的衰老时钟分析显示,维生素C显著降低大脑、皮肤、肾脏等器官的生物学年龄,并在海马和胰腺中逆转特定细胞类型的衰老程序。脑部MRI表明,维生素C可抵抗脑结构退变、改善连接完整性;代谢指标显示胰岛素抵抗和血脂异常得到缓解。
该研究系统阐释了铁-ACSL4-脂质过氧化这一程序化衰老轴心,并揭示其与NRF2等抗氧化防御系统之间的拮抗关系;建立了量化该过程的分子标志物体系,鉴定出核心调控靶点ACSL4,并在此基础上探索了基因治疗与小分子药物两种干预策略,形成了从机制解析到干预验证的完整研究闭环。该通路在不同分裂能力细胞中普遍存在,且从啮齿类到灵长类呈现进化保守性,提示铁衰老可能是哺乳动物衰老的一种共性机制。
在转化应用层面,该研究提供了两种互补的干预路径:一是基于CRISPR的ACSL4基因治疗,代表精准长效干预方向;二是维生素C作为直接ACSL4抑制剂,代表安全可及的日常干预策略。两条路径均指向铁衰老这一驱动多器官功能衰退的内在程序,为神经退行性疾病、代谢性疾病及心血管疾病的预警与干预提供了全新切入点。
围绕铁衰老这一新概念,仍有诸多科学问题有待解答,包括:ACSL4在不同细胞类型及衰老相关疾病中的精细调控机制;基因治疗与小分子干预的长期安全性;维生素C剂量与个体遗传背景对疗效的影响;循环中铁衰老标志物用于衰老度量与疾病预警的价值;以及长期铁摄入过量是否可能加速人体衰老进程及其临床相关性等。对这些问题的持续追问,将逐步深化人类对衰老复杂性的认知。
文章链接:https://doi.org/10.1016/j.cmet.2026.02.010
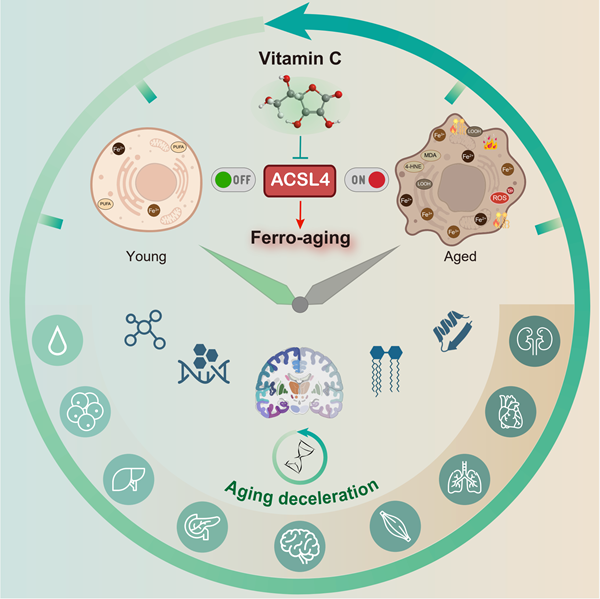
铁衰老——衰老及退行性疾病干预新靶标
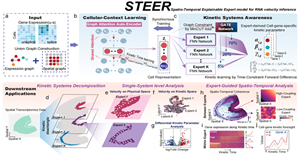
在复杂生命系统中,细胞状态会随着发育、组织重塑和疾病演化不断变化。RNA速度分析(RNA velocity)为从静态转录组数据中推断细胞状态演进趋势提供了重要手段。然而,在真实生物组织中,往往存在多种细胞动态过程...
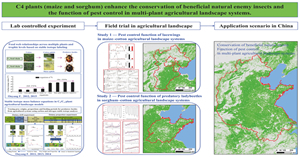
植物是生态系统中物质和能量循环的核心组成部分,并支撑整个生态系统的运转。在国家重点研发计划“区域生态产品核算技术方法与价值实现机制”项目的支持下,中国科学院动物研究所欧阳芳负责的 “典型农田生态系统...
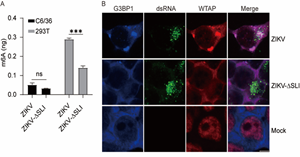
虫媒病毒如登革病毒、寨卡病毒在世界范围内流行,给人类健康和生物安全带来巨大挑战。这类病毒通过节肢动物媒介叮咬这一特殊方式在媒介-宿主之间进行传播。虫媒病毒必须在节肢动物媒介和脊椎动动物宿主之间交替感...

